Koolstofchemie
Koolstof
Je kan op basis van de Bohrmodellen en de Lewis dot structuren de structuur van koolwaterstoffen verklaren en tekenen. Je kent de belangrijkste isomeren en functionele groepen.
LEERDOELEN
- Je kan het Bohr model en de Lewis dot structuur van koolstof, zuurstof, stikstof en waterstof tekenen en begrijpt de implicaties hiervan voor de onderlinge atoombindingen.
- Je kent de structuur van eenvoudige koolwaterstoffen en kan deze tekenen.
- Je kent drie vormen van isomeren (structurele isomeren, cis-trans isomeren en enantiomeren) en kan deze tekenen.
- Je kent het begrip functionele groepen en kent degene die staan aangegeven in tabel 3.6
CARBON ATOMS CAN FORM ….
Lees en bestudeer: The formation of bonds with carbon. Je ziet dat koolstof 4 bindingen kan maken; waterstof 1; zuurstof 2 en stikstof 3. Je kan dit ook zien in de figuur (zie e-book) waarin de bindingen met elektronen volgens het lewis stuctuurmodel worden getoond.
Lees en bestudeer: Molecular diversity ….tot isomeren
Je ziet dat de structuur vooral van de 4 bindingen van C de mogelijkheid biedt voor een range aan moleculen, hier de zogenaamde koolwaterstoffen (hydrocarbons)
LD1 en LD2
Zie ook de figuur voor representaties van methaan, ethaan en etheen.
Zie figuur “four ways that carbon …”: vormen van moleculen
een leuk filmpje over de diversiteit van moleculen met koolstof:
Lees en bestudeer: Isomeren. Probeer met behulp van de figuur de drie hoofdgroepen van isomeren te begrijpen
LD3
In de les neem ik een molecuulbouwdoos mee, zodat je de isomeren ook in 3D kan bestuderen.
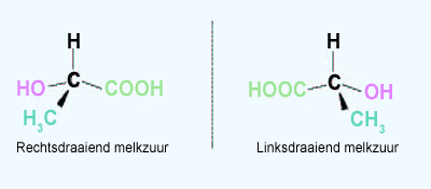
Lees en bestudeer Chemical groups. en functional groups.
Kijk ook alvast even naar ATP
LD4
Leer de functionele groepen van Figuur 3.6 uit je hoofd. Zorg dat je ze kan herkennen in tekeningen van de moleculen en onthoud ook de voorbeelden.